中大新聞中心
中大研究團隊開發多功能納米探針 監察柏金遜病病變 有望緩解病情惡化
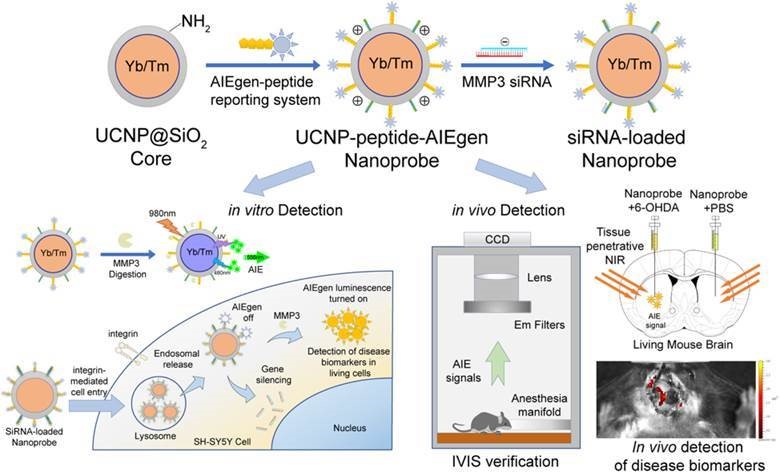
香港中文大學(中大)工程學院生物醫學工程學系邊黎明教授和中大醫學院生物醫學學院及蔡永業腦神經科學中心容永豪教授及柯亞教授領導的研究團隊最近研發了一種多功能納米探針,可用於察柏金遜病進展,有助預防病情進一步惡化。該科研成果目前已於美國化學學會《應用材料與界面》(ACS Applied Materials and Interfaces)期刊發表。
柏金遜病是一種主要發病於老年人的神經退化性疾病,可分為原發性和誘發性兩類,其中大部分是原發性,主要是由於腦內部分神經系統功能受損,不能製造一種稱為多巴胺的神經傳導物質。當腦部缺乏多巴胺,信息不能正常從神經細胞傳送至肌肉,就會出現震顫、僵硬和遲緩等柏金遜病徵狀。現階段其明確成因仍未有一致的結論。
愈來愈多證據顯示,柏金遜病患者腦中會過度產生基質金屬蛋白酶(MMPs), 其中MMP3可引發多巴胺能神經元凋亡,產生神經炎症,令患者出現柏金遜病症狀。研究人員發現,MMP 3抑制劑可有效減少炎症性小膠質細胞活化和多巴胺能神經元死亡,證實MMP3可成為有效的早期柏金遜病生物標誌物和臨床干預的標靶。邊黎明教授認為,如利用一種多功能納米探針來指示並抑制大腦中MMP 3的異常活動,有望及早發現柏金遜病和其他神經退化性疾病的症狀,在疾病初期延緩病情惡化。
診療柏金遜病多功能納米探針的開發
治療PD的主要挑戰之一是有效檢測和抑制早期MMP3活性,以減輕神經應激和炎症反應。2018年初,邊黎明教授科研團隊中的博士研究生李睿和博士後研究員黎錦明博士合作研發了一種酶響應納米探針,可用於監測神經退化性疾病的生物標誌物。其後,邊教授團隊與容永豪教授及柯亞教授科研團隊的李怡博士等人合作,進一步改良這種納米探針,設計出專用於監測柏金遜病生物標誌物活性並同時遞送治療劑的多功能納米探針。在實驗室驗證成功後,研究小組與威爾斯親王醫院的李郁偉教授合作,在小鼠柏金遜病模型中進一步驗證納米探針的功效。納米探針在患有柏金遜病的小鼠大腦中可顯示出明顯的熒光信號,首次成功於活體動物大腦中進行MMP 3的活性監測,證明該納米探針在監測腦細胞應激和腦組織炎症反應、診斷早期柏金遜病的應用當中極具潛力。
邊黎明教授表示:「研究小組未來將著重於改良探針的使用方法,並且負載更為有效的治療劑以達到治療神經退化性疾病的最佳效果,提高納米探針的臨床適用性。」
容永豪教授表示:「PD只是影響大腦的許多神經退化性疾病之一。我們希望將該技術擴展及應用到其他腦部疾病。」
上述科研得到中國國家自然科學基金、香港醫療衞生研究基金、香港研究資助局優配研究金、中大周毓浩創新醫學技術中心及中大蔡永業腦神經科學中心的資金支持。