中大新聞中心
中大揭示幽门螺旋杆菌在人体胃部存活之秘拓新方案以灭绝引致胃溃疡及胃癌之元凶
香港中文大学(中大)生命科学学院蛋白质科学与晶体研究中心黄锦波教授及其研究团队最近发表一项研究结果,揭示了幽门螺旋杆菌(Helicobacter pylori)如何在人体胃部的酸性环境中生存。幽门螺旋杆菌可引致消化性溃疡甚至胃癌,现时全球已有一半人口受感染。此项研究成果有助研发治疗幽门螺旋杆菌感染的新药物,获选为学术期刊Journal of Biological Chemistry的「本周最佳论文」。
幽门螺旋杆菌是已知唯一能在胃酸中生长的细菌,它会损害肠道黏膜,导致消化性溃疡及引起胃炎。现有的抗生素可以治愈八至九成由病菌引致的溃疡,但随着幽门螺旋杆菌的抗药性与日俱增,抗生素会逐渐失效,故必须及早开发新的药物来对抗幽门螺旋杆菌的感染。
黄锦波教授的研究生方宇亨同学指出,幽门螺旋杆菌能在胃酸中生存,是由于它可生产尿素酶以分解在胃内的尿素,使之释放出氨,从而中和胃酸。然而,与其他大多数酶不同的是,尿素酶由病菌产生后,不可直接发挥其作用;它需要接收到两个镍离子以后,才可转化为有活性的酶。
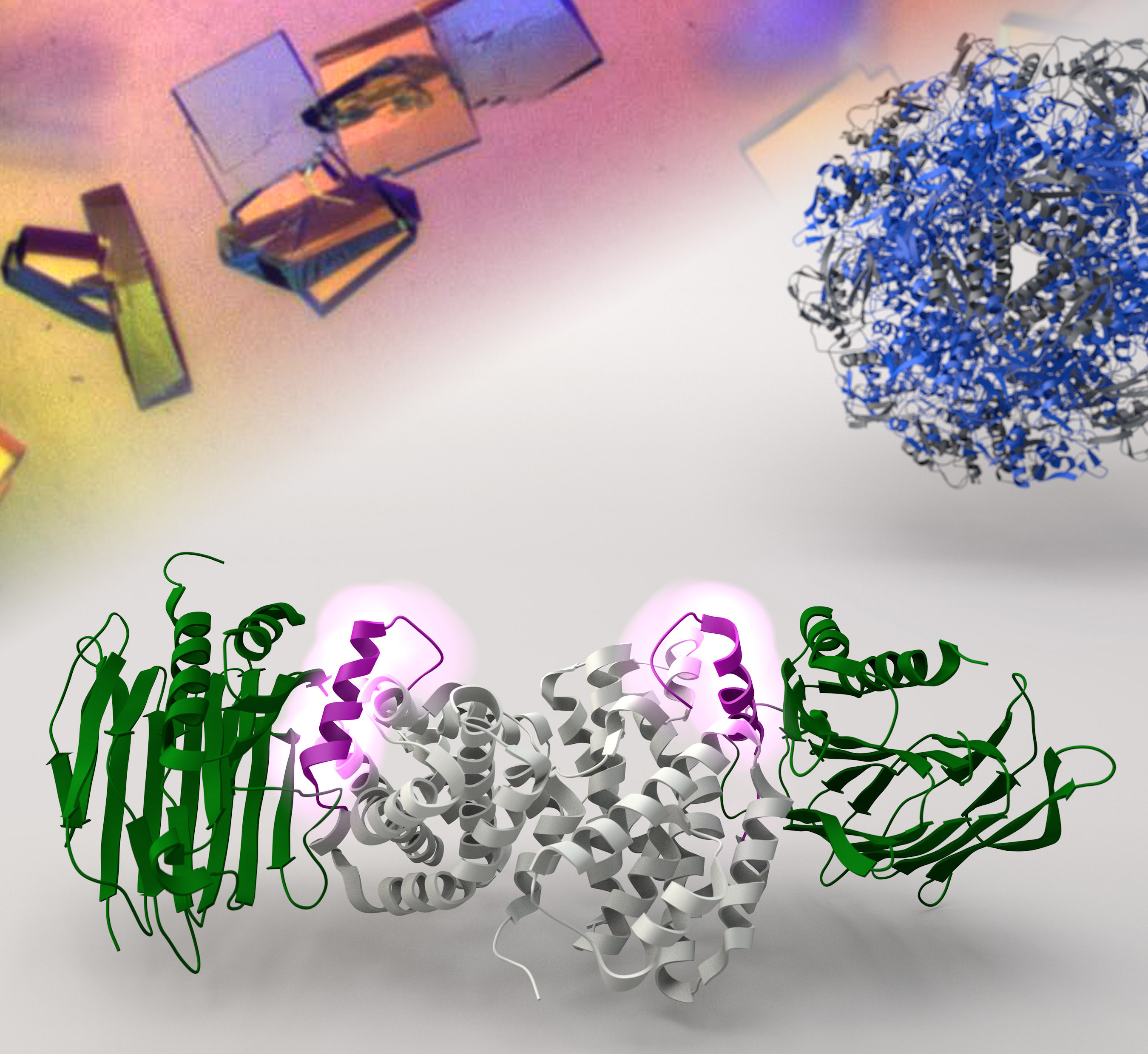
「由于幽门螺旋杆菌的生存取决于有活性的尿素酶,因此对病菌而言,镍离子能否运送到尿素酶实属生死攸关的事。」黄教授说。他的团队便致力研究四个辅助激活尿素酶的蛋白质:UreE、UreF、UreG和UreH。他们利用X射线晶体学技术,产生像显微镜一样的效果,以观察蛋白质的分子结构。他们发现了UreF、UreH和UreG这三个辅助蛋白如何自行集结成一个分子机器,将镍离子运送到尿素酶。镍离子一旦到位,尿素就会被分解为氨,从而中和胃酸。
更重要的是,他们证实了破坏UreF-UreH-UreG分子机器的形成能抑制活性尿素酶的合成。「现在我们知道这分子机器是如何进行自我组装,就能想办法把它拆解。由于活性的尿素酶是幽门螺旋杆菌赖以生存的关键,以这个分子机器为标靶而开发的药物,很有可能是根除致病菌的新策略。」黄教授说。根据这些发现,研究小组正在设计新药以抑制该分子机器的自我组装,灭绝幽门螺旋杆菌在胃酸中存活的机会。